Кратко о танинах…
Добрый день, уважаемые читатели. Сегодня мы поговорим с вами о танинах, их применении и некоторых свойствах.
Итак, танины (таннины) — это группа фенольных соединений растительного происхождения, содержащих в своём составе большое количество гидроксильных групп (-ОН).
Все существующие танины можно разделить на 2 большие группы: гидролизуемые танины и конденсированные танины. К первой группе (гидролизуемым танинам) относятся вещества, образованные многоатомным спиртом с частичной или полной этерификацией гидроксильных групп галловой кислотой (либо родственными ей соединениями). Ко второй группе (конденсированным танинам) относятся вещества, образованные конденсацией фенольных соединений.
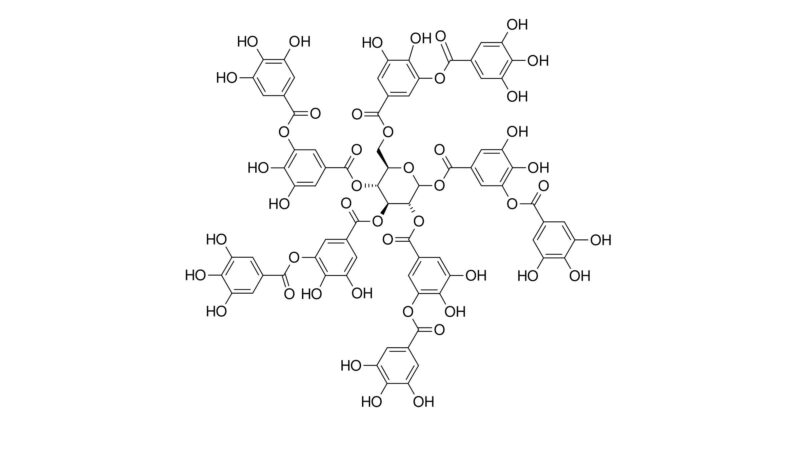
В подборке фото ниже приведены структурные формулы галловой кислоты, галлотанина (гидролизуемый танин), флаван-3-ола и процианидина С1 (конденсированный танин).
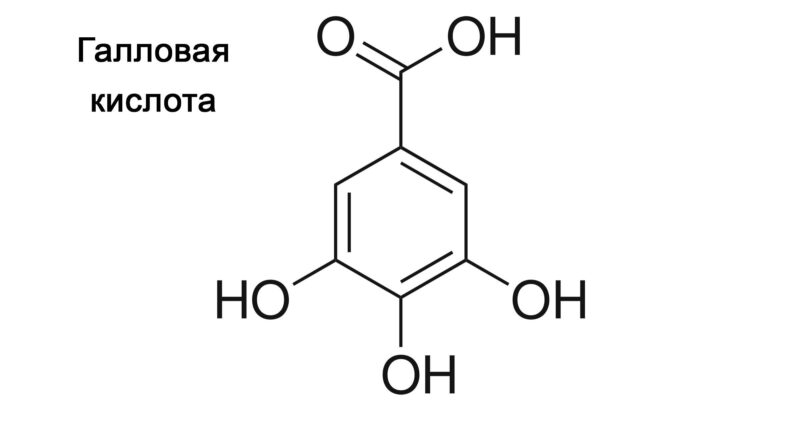
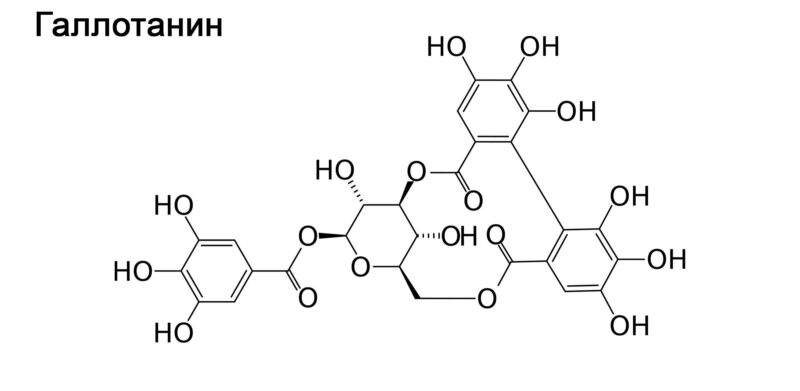
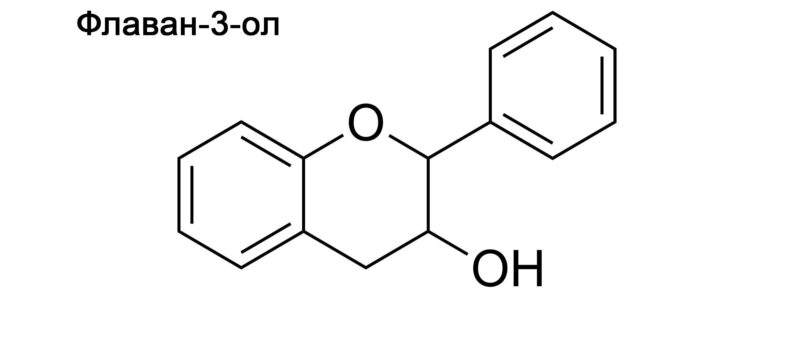
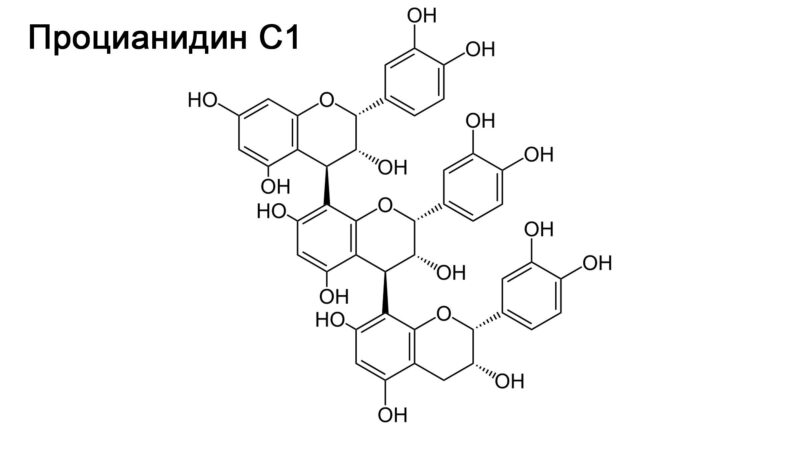
Все танины обладают дубильными свойствами в связи с чем в промышленности используются для дубления кожи и меха. Кроме того танины используют при производстве чернил и протравливания текстильных волокон. В аналитической химии танины нашли применение при качественной идентификации некоторых металлов (в частности железа). В медицине танины используются в качестве вяжущего средства.
В природе танины встречаются повсеместно — в ягодах, орехах, травах… …достаточно много танинов содержит кора дуба, каштана, акации… …плоды хурмы, черёмухи, каштана… Именно танины придают им терпкий вяжущий вкус.
Одной из распространённых форм танинов является дубильная (галлодубильная, таниновая) кислота, получаемая из чернильных орешков — наростов на молодых побегах малоазиатского дуба, скумпии и пр. Физически представляет из себя светло-желтый или буровато-желтый аморфный порошок со слабым своеобразным запахом и вяжущим вкусом. Легко растворима в спирте и воде. Именно с ней мы сегодня в основном и будем проводить наши эксперименты.
Внешний вид и структурная формула дубильной кислоты приведены в подборке фото ниже.

1. Для проведения первого опыта необходимо в 100-120 мл воды растворить 0.1-0.2 г. хлорида железа(III). Если к полученному раствору по каплям приливать 0.5% водный раствор дубильной кислоты, то раствор окрасится в насыщенный сине-чёрный цвет.
Вживую это выглядит вот так:
Фактически данная реакция является качественной на фенольный гидроксил. В данном опыте вместо хлорида железа(III) можно воспользоваться железоаммонийными квасцами. При этом гидролизуемые танины дадут сине-чёрное окрашивание, а конденсированные зелёно-чёрное.
2. Для проведения второго опыта необходимо взять заваренный чёрный чай и налить в 2 стакана по 80-120 мл. Если теперь в один стакан прилить 5% раствор серной кислоты, а во второй 5% раствор гидроксида натрия, то хорошо видно изменение цвета раствора в обеих стаканах. В стакане с добавлением серной кислоты раствор стал более светлым, а в стакане с гидроксидом натрия — более тёмным.
Вживую это выглядит вот так:
Дело в том, что золотисто-красноватый цвет чая обусловлен в основном присутствующими в составе танинами. Некоторые танины являются природными индикаторами pH. Именно по этой причине чай светлеет при добавлении в него лимона. И именно этим пользуются некоторые продавцы чая, подщелачивая разбавленный напиток.
Для проведения опыта вместо серной кислоты можно использовать лимонную, винную, уксусную. А вместо гидроксида натрия можно воспользоваться гидрокарбонатом натрия (пищевой содой).
3. Для проведения третьего опыта необходимо растворить 0.2-0.3 г. перманганата калия в 100-120 мл тёплой воды и подкислить раствор 3-5 мл 30% раствора серной кислоты. Если к такому раствору по каплям приливать 1-3% водный раствор дубильной кислоты, то цвет раствора изменится на светло-жёлтый.
Вживую это выглядит вот так:
Дело в том, что фенольные ОН-группы танинов достаточно легко окисляются перманганатом калия до продуктов, имеющих жёлтый цвет.
4. Для проведения четвёртого опыта необходимо 2-3 г желатина растворить в горячей воде. Если к полученному раствору прилить 1-3% раствор дубильной кислоты, то в растворе выпадет вязкий эластичный осадок.
Вживую это выглядит вот так:
Дело в том, что танин способен сворачивать (свёртывать) белки, а желатин — частично гидролизованный белок коллаген. На этом свойстве танинов как раз и основан процесс дубления.
5. Для проведения пятого опыта необходимо измельчить и растворить в 100-120 мл теплой воды 2-3 таблетки лекарственного средства анальгин-хинин. Далее необходимо отфильтровать выпавший на дно нерастворимый осадок (остатки нерастворившегося метамизола натрия). Получится раствор с небольшим зеленоватым оттенком. Оттенок раствора обусловлен красителем, содержащемся в оболочке таблеток.
Если к полученному раствору по каплям приливать 1-3% раствор дубильной кислоты, то в растворе выпадет белый осадок. Вживую это выглядит вот так:
Суть в том, что лекарственный препарат анальгин-хинин содержит в своём составе соль алкалоида — хинина гидрохлорид. Соли алкалоидов осаждают танины из раствора — образуется белый осадок.
6. Для проведения шестого опыта необходимо растворить 5 г. дихромата калия (дихромата натрия) в 100-120 мл теплой воды. Если к такому раствору по каплям приливать 1-3% раствор дубильной кислоты, то в растворе выпадет коричневый осадок (либо образуется коричневая муть).
Вживую это выглядит вот так:
Выпадение осадка при взаимодействии танина с дихроматом калия (дихроматом натрия) — гистохимическая реакция на танины.
7. Если же в предыдущем опыте использовать не дихромат калия (дихромат натрия), а раствор хромового ангидрида в воде (т.е. фактически раствор хромовых кислот), либо хромовую смесь (раствор хромового ангидрида в серной кислоте), то результат опыта получится совсем иным.
Для проведения седьмого опыта необходимо 5 г. хромового ангидрида растворить в 100-120 мл воды (либо 30-40% раствора серной кислоты). Если к такому раствору по каплям приливать 1-3% раствор дубильной кислоты, то изначально в растворе выпадет черно-коричневый осадок, растворяющийся со временем при перемешивании.
Вживую это выглядит вот так:
Суть в том, что даже при такой небольшой концентрации хромовые кислоты, а в особенности хромовая смесь являются достаточно сильными окислителями (именно это свойство используется при очистке химической лабораторной посуды от органических загрязнений). При окислении танина образуются продукты, окрашенные в коричнево-черный цвет.
При этом раствор в случае использования хромовой смеси приобретает дополнительно зеленоватый оттенок вследствие образования сульфата хрома(III). При использовании же чистого хромового ангидрида зеленоватый оттенок обусловлен образованием оксида хрома(III).
Опыт необходимо проводить осторожно и в вытяжном шкафу т.к. процесс окисления экзотермический, а хромовый ангидрид относится к 1 классу опасности.
Вот такие интересные вещества танины.
А на этом на сегодня всё. Спасибо, что дочитали до конца!
Список использованной литературы:
2. М.Н. Запромётов, «Основы биохимии фенольных соединений», изд-во «Высшая школа», Москва, 1974 г., 214с.
3. А.А. Орлова, М.Н. Повыдыш. Обзор методов качественного и количественного анализа танинов в растительном сырье. Химия растительного сырья, 2019, №4, с. 29–45.
4. Н. С. Зефиров, Н. Н. Кулов и др. Химическая энциклопедия. — М.: Научное издательство «Большая российская энциклопедия», 1995. — Т. 4. — С. 493—494.
5. Коноплева М.М. Фармакогнозия: природные биологически активные вещества/Витебск: Витебский государственный медицинский университет, 2010. — 234 с.